Европейската агенция по лекарствата (EMA) започва преглед в реално време на експерименталното лекарство срещу коронавирус за възрастни на американските фармацевтични компании Merck и Ridgeback, съобщава "Ройтерс".
Процедурата, известна още като "непрекъснат преглед", означава, че европейският регуратор ще оцени даннитe веднага щом станат достъпни, а няма да чака официално заявление, когато бъде събрана цялата необходима информация.
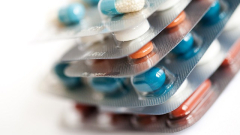
Към момента ваксините са основното оръжие срещу COVID-19. Експерименталното хапче "молнупиравир" (molnupiravir) обаче може да промени хода на борбата с вируса, след като от проучвания стана ясно, че то може да намали наполовина вероятността от смърт или хоспитализация за най-застрашените от тежко преболедуване.
На 11 октомври компанията Merck подаде заявление за разрешение за спешна употреба на лекарството в САЩ. Предстои групата от външни съветници на американския здравен регулатор да обсъди в края на ноември дали да разреши експерименталното хапче.
В случай че "молнупиравир"-ът бъде одобрен от регулаторните органи, той ще се превърне в първото лекарство за лечение на коронавирус, прилагано през устата. Освен това той ще осигури първото лечение на пациенти с леки заболявания, за разлика от съществуващите лекарства, които се използват най-вече за лечение на критично болни.
Производителят на лекарства има договор с американското правителство за доставка на 1,7 милиона курса от това лекарство на цена от 700 долара за курс. Наскоро Merck подписа договори за доставки и с редица други страни, сред които Великобритания, Малайзия и Сингапур.
ЕС също обмисля подписването на споразумение за доставка на антивирусното хапче. Това обаче може да се случи едва след като компанията започне процеса на искане на одобрение за лекарството.












































 USD
USD CHF
CHF GBP
GBP